《制取氧氣》
一、VR教學目標
1、知識與技能
(1). 了解分解過氧化氫制取氧氣的方法和原理。
(2). 了解二氧化錳在過氧化氫分解中的作用;歸納認識催化劑的概念與作用。
2、過程與方法
(1)學會運用實驗、觀察等方法獲取信息。
(2)能主動與他人進行交流與討論,表達自己的觀點,逐步形成良好的學習方法和學習習慣,培養學生分析及推理能力。
3、情感態度與價值觀
讓學生在寬松、愉悅中學習,增強學生進行科學探究的欲望和激情;培養學生正確應用科學知識生活。
二、教學重點與難點
1、教學重點
(1). 過氧化氫制取氧氣
(2). 分解反應
2、教學難點
催化劑的概念與特點
三、VR教學過程
1、新課導入
“氧來樂”是養魚伯伯的“救命藥”,魚塘內定期使用可避免魚兒缺氧死亡。
【主要成分】過氧化氫
【含量規格】15%
【作用與用途】
本品在分解過程中釋放出活潑的新生態氧,用于養殖池塘的增氧,藥性溫和,使用方便,分解快,無殘留,綠色環保。
【用法與用量】
用法:將本品以1000倍水稀釋后直接潑灑于養殖池塘中。
用量:每畝水深1米用本品100~150ml,病情嚴重可加量使用
我們進入化學實驗室探究過氧化氫是如何分解放出氧氣的?
2、催化劑的特點
【教師】過氧化氫溶液在常溫下分解就可放出氧氣,通常還加入二氧化錳,這是為什么呢?
【學生】猜測原因
【教師】實驗演示
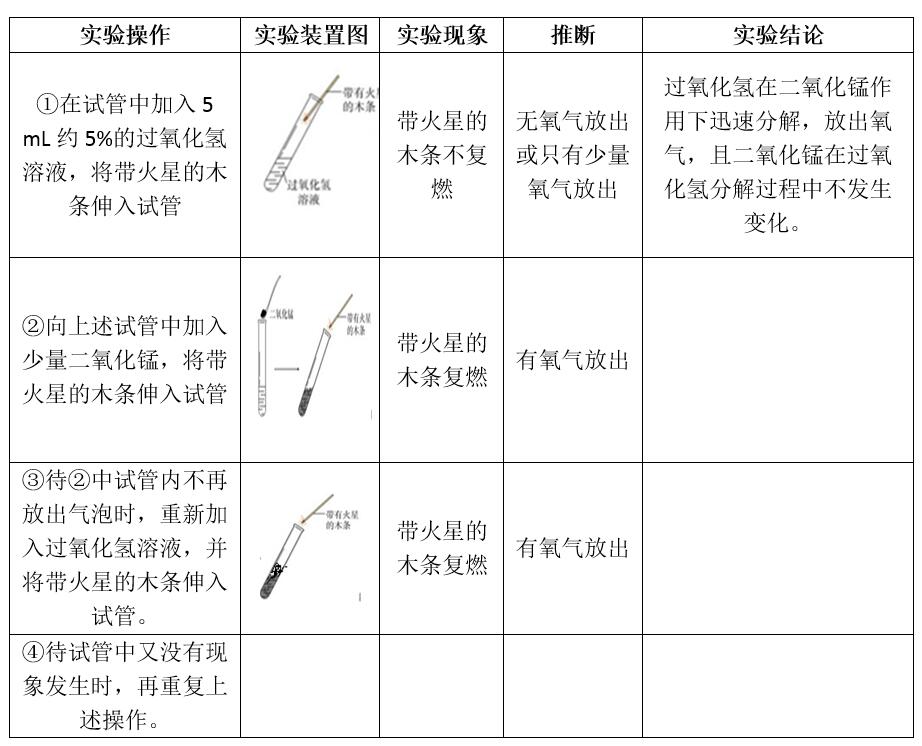
【教師】上述實驗中二氧化錳分解放出氧氣嗎?二氧化錳在此反應中起什么作用?
【學生】在過氧化氫分解的過程中,二氧化錳好像永遠用不完。
【教師】將反應后的混合物過濾、洗凈、干燥、稱量,會發現反應后的二氧化錳與反應前的二氧化錳質量相等,且化學性質不變。在化學反應中能改變其他物質的反應速率,而本身的質量和化學性質在化學反應前后沒有改變的物質叫催化劑(又叫觸媒)。催化劑在化學反應中所起的作用叫催化作用。
知識拓展
催化劑的理解及注意事項:
①催化劑的特點:“一變兩不變”。“一變”是指“能改變化學反應速率”;包括加快和減慢兩個方面。“兩不變”是指“催化劑的質量和化學性質”在化學變化前后不發生改變;是“化學性質”而不是“性質”。
②催化作用的結果只影響反應速率,并不能增加或減少生成物的質量,生成物的質量只與反應物的質量有關。
③催化劑是參加化學反應的,催化劑的質量和化學性質在化學變化前后不發生改變,但在化學反應過程中可能會改變。催化劑雖然可以參加化學反應過程,但催化劑不是反應物。
④催化劑是針對某反應而言的。如二氧化錳在過氧化氫分解制取氧氣的過程中,能夠起催化作用;但二氧化錳不是所有化學反應的催化劑。
⑤催化劑不是萬能的,也不是唯一的。對某一反應,可以選擇不同的物質作為催化劑。如過氧化氫分解制取氧氣時,既可以選擇二氧化錳做催化劑,也可以選擇氧化鐵等做催化劑。
3、過氧化氫分解制取氧氣
【教師】請同學們閱讀課本,總結如何在實驗室中通過分解過氧化氫的方法制取氧氣?反應的原理是什么?
【學生】
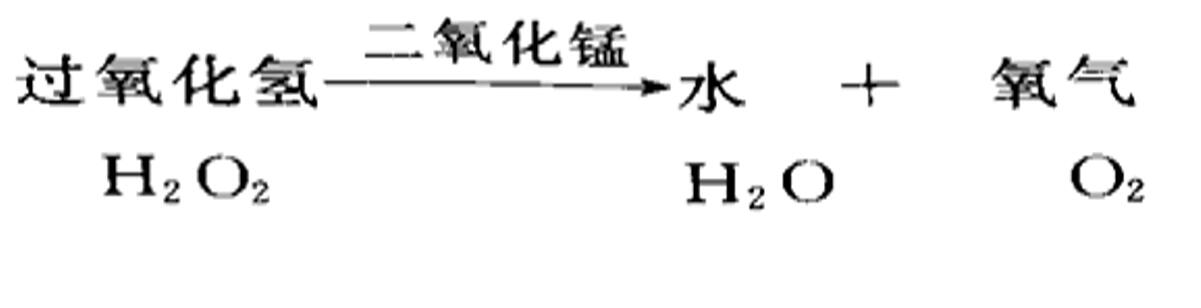
【教師】那么我們在實驗室中應該用什么樣的裝置,按照怎樣的順序來進行實驗呢?帶著這些問題,我們來看一個視頻并填寫表格。
【學生】觀看VR互動教學視頻-過氧化氫制取氧氣,觀看后小組交流總結,填寫表格,匯報。
實驗裝置的名稱 | |
實驗步驟 | |
實驗現象 | |
微觀現象 |

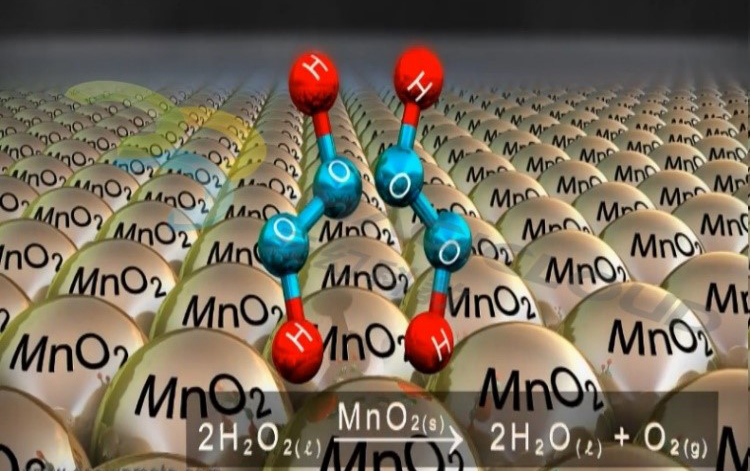
【教師】對實驗進行總結
四、板書設計
第二單元 我們周圍的空氣
課題3 制取氧氣
二、過氧化氫制取氧氣
1、反應原理
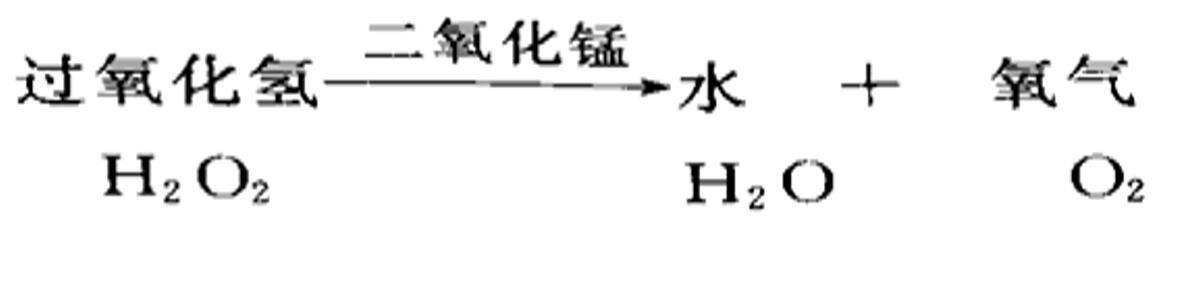
2、反應裝置:固-液不加熱型
收集裝置:排水法
三、催化劑——一變兩不變
變:改變反應速率
不變:本身的質量和化學性質不變